MG0010試験:有効性
国際共同第Ⅲ相二重盲検試験(MG0010試験[検証的試験])
- 社内資料
- 国際共同第Ⅲ相二重盲検試験成績 MG0010試験(承認時評価資料)
Howard JF Jr. et al.: Lancet Neurol. 2023; 22(5): 395-406.
(本試験はUCB Pharmaの資金提供を受けており著者に同社より研究資金や謝礼等を受領している者が含まれる)
主要評価項目:12週におけるMG-ADL総スコアのベースラインからの変化量
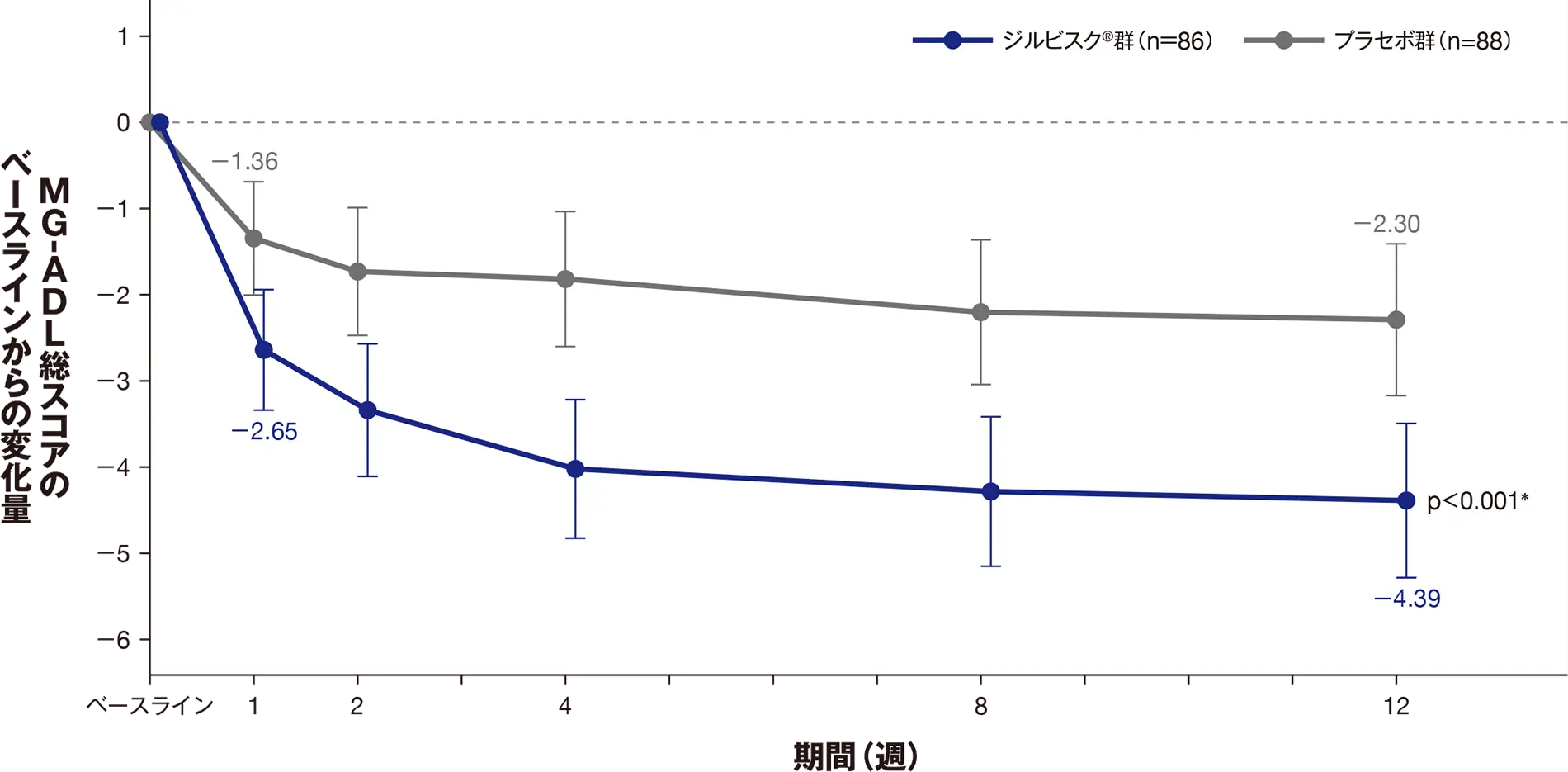
主要評価項目である12週におけるMG-ADL総スコアのベースラインからの変化量の最小二乗(LS)平均値は、ジルビスクⓇ群-4.39、プラセボ群-2.30であり、ジルビスクⓇ群のプラセボ群に対する優越性が検証されました[LS平均値の差:-2.09、p<0.001(MMRM ANCOVAモデル解析)]。
ジルビスクⓇ群では、投与1週からMG-ADL総スコアの低下がみられ[ベースラインからの変化量のLS平均値(95%CI):-2.65(-3.34~-1.96)]、12週において臨床的に意義のある改善が示されました※。
- ※
- 眼、球、呼吸器及び体幹症状にわたる8項目の症状及び障害を対象とし、個々の項目への回答を合計することで得られるMG-ADL総スコアは0~24であり、スコアが高いほど障害の程度が重いことを示す1)。MG-ADLの2点の低下は臨床的に意義のある改善を示す2)。
| ジルビスクⓇ群(n=86) | プラセボ群(n=88) | |
|---|---|---|
| LS平均値±SE(95%CI) | -4.39±0.45(-5.28~-3.50) | -2.30±0.44(-3.17~-1.43) |
| LS平均値の群間差±SE(95%CI) | -2.09±0.58(-3.24~-0.95) | ― |
| p値 | <0.001* | ― |
- *
- 治験薬、治験薬と来院の交互作用項、ベースラインのMG-ADL及びQMG総スコア、地理的地域、並びにベースラインのMG-ADL総スコアと来院の交互作用項を固定効果、患者を変量効果としたMMRM ANCOVAモデル解析
- *
- 治験薬、治験薬と来院の交互作用項、ベースラインのMG-ADL及びQMG総スコア、地理的地域、並びにベースラインのMG-ADL総スコアと来院の交互作用項を固定効果、患者を変量効果としたMMRM ANCOVAモデル解析
重要な副次評価項目:12週におけるQMG総スコアのベースラインからの変化量
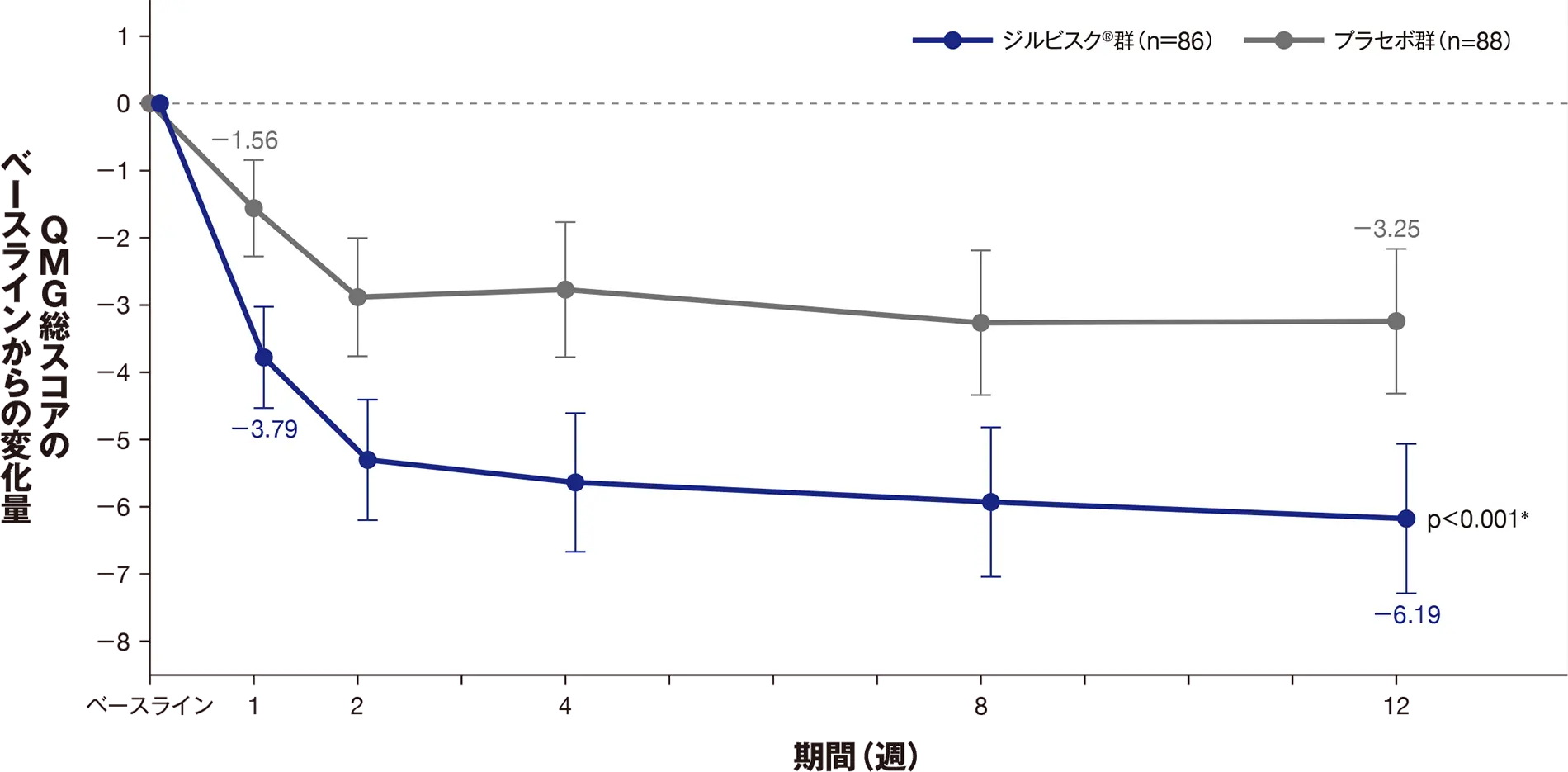
12週におけるQMG総スコアのベースラインからの変化量のLS平均値は、ジルビスクⓇ群-6.19、プラセボ群-3.25であり、ジルビスクⓇ群でプラセボ群に対して統計学的に有意な低下が見られました[LS平均値の差:-2.94、p<0.001(MMRM ANCOVAモデル解析)]。
ジルビスクⓇ群では、投与1週からQMG総スコアの低下がみられ[ベースラインからの変化量のLS平均値(95%CI):-3.79(-4.54~-3.03)]、12週において臨床的に意義のある改善が示されました※。
- ※
- QMGスコアは、眼、顔面筋力、嚥下、発話、四肢筋力、努力肺活量(FVC)などの13項目を検査し、機能及び構造の障害に基づき疾患の重症度を定量化する3, 4)。総スコアは0~39であり、スコアが高いほど疾患の重症度が高いことを示す。3点の変化を臨床的に意義があるとみなす5,6)。
| ジルビスクⓇ群(n=86) | プラセボ群(n=88) | |
|---|---|---|
| LS平均値±SE(95%CI) | -6.19±0.56(-7.29~-5.08) | -3.25±0.55(-4.32~-2.17) |
| LS平均値の群間差±SE(95%CI) | -2.94±0.73(-4.39~-1.49) | ― |
| p値 | <0.001* | ― |
- *
- 治験薬、治験薬と来院の交互作用項、ベースラインのMG-ADL及びQMG総スコア、地理的地域、並びにベースラインのQMG総スコアと来院の交互作用項を固定効果、患者を変量効果としたMMRM ANCOVAモデル解析
- *
- 治験薬、治験薬と来院の交互作用項、ベースラインのMG-ADL及びQMG総スコア、地理的地域、並びにベースラインのQMG総スコアと来院の交互作用項を固定効果、患者を変量効果としたMMRM ANCOVAモデル解析
重要な副次評価項目:12週におけるMGC総スコアのベースラインからの変化量
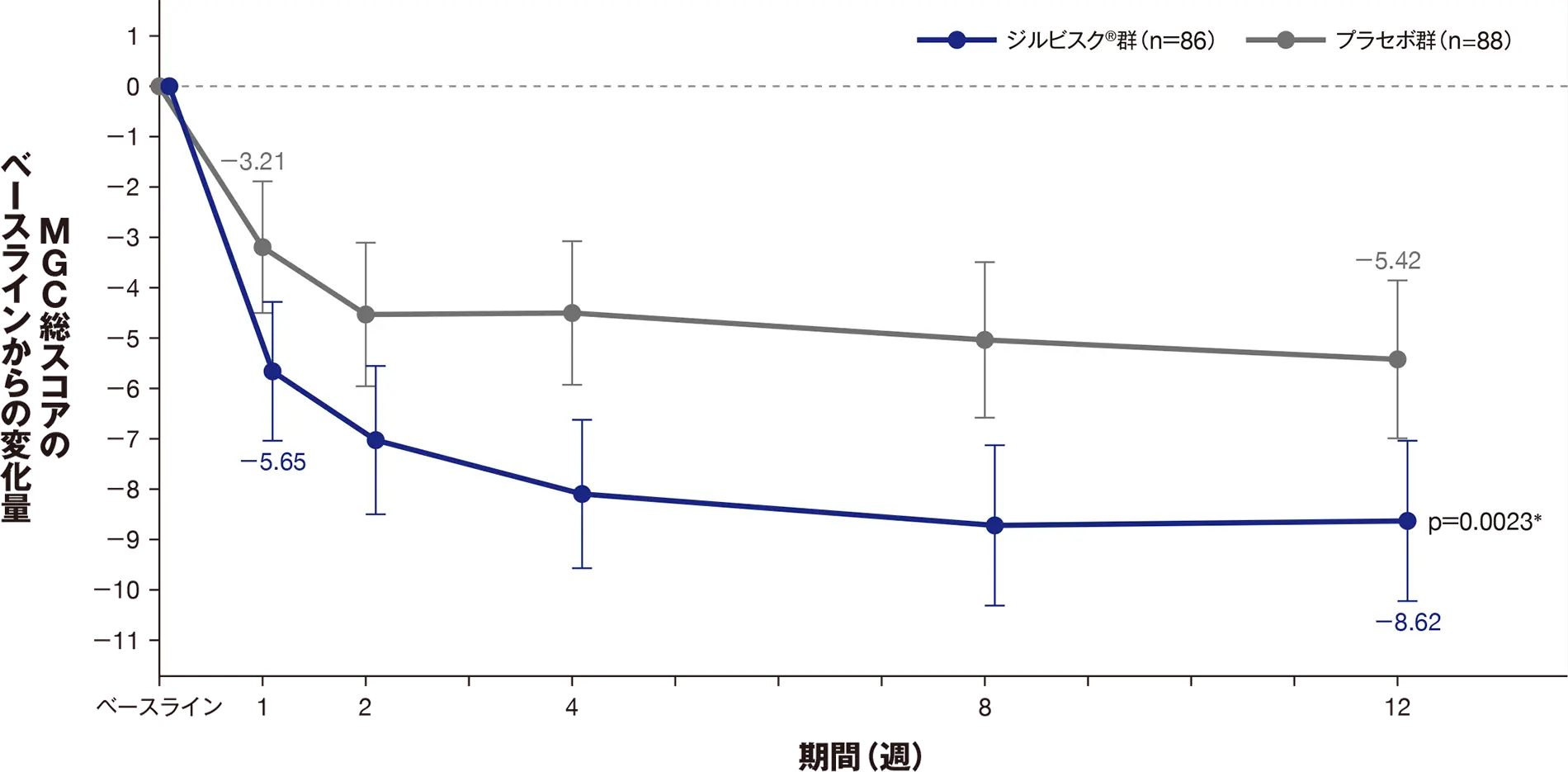
12週におけるMGC総スコアのベースラインからの変化量のLS平均値は、ジルビスクⓇ群-8.62、プラセボ群-5.42であり、ジルビスクⓇ群でプラセボ群に対して統計学的に有意な低下が見られました[LS平均値の差:-3.20、p=0.0023(MMRM ANCOVAモデル解析)]。
ジルビスクⓇ群では、投与1週からMGC総スコアの低下がみられ[ベースラインからの変化量のLS平均値(95%CI):-5.65(-7.02~-4.28)]、12週において臨床的に意義のある改善が示されました※。
- ※
- MGCスコアは、医師による検査及び患者の病歴に基づく10項目のMG症状及び徴候の評価指標である。総スコアは0~50となり、スコアが高いほど疾患の重症度が高いことを示し、3点の変化が臨床的に意義のある変化となる7)。
| ジルビスクⓇ群(n=86) | プラセボ群(n=88) | |
|---|---|---|
| LS平均値±SE(95%CI) | -8.62±0.81(-10.22~-7.01) | -5.42±0.79(-6.98~-3.86) |
| LS平均値の群間差±SE(95%CI) | -3.20±1.03(-5.24~-1.16) | ― |
| p値 | 0.0023* | ― |
- *
- 治験薬、治験薬と来院の交互作用項、ベースラインのMG-ADL、QMG及びMGC総スコア、地理的地域、並びにベースラインのMGC総スコアと来院の交互作用項を固定効果、患者を変量効果としたMMRM ANCOVAモデル解析
- *
- 治験薬、治験薬と来院の交互作用項、ベースラインのMG-ADL、QMG及びMGC総スコア、地理的地域、並びにベースラインのMGC総スコアと来院の交互作用項を固定効果、患者を変量効果としたMMRM ANCOVAモデル解析
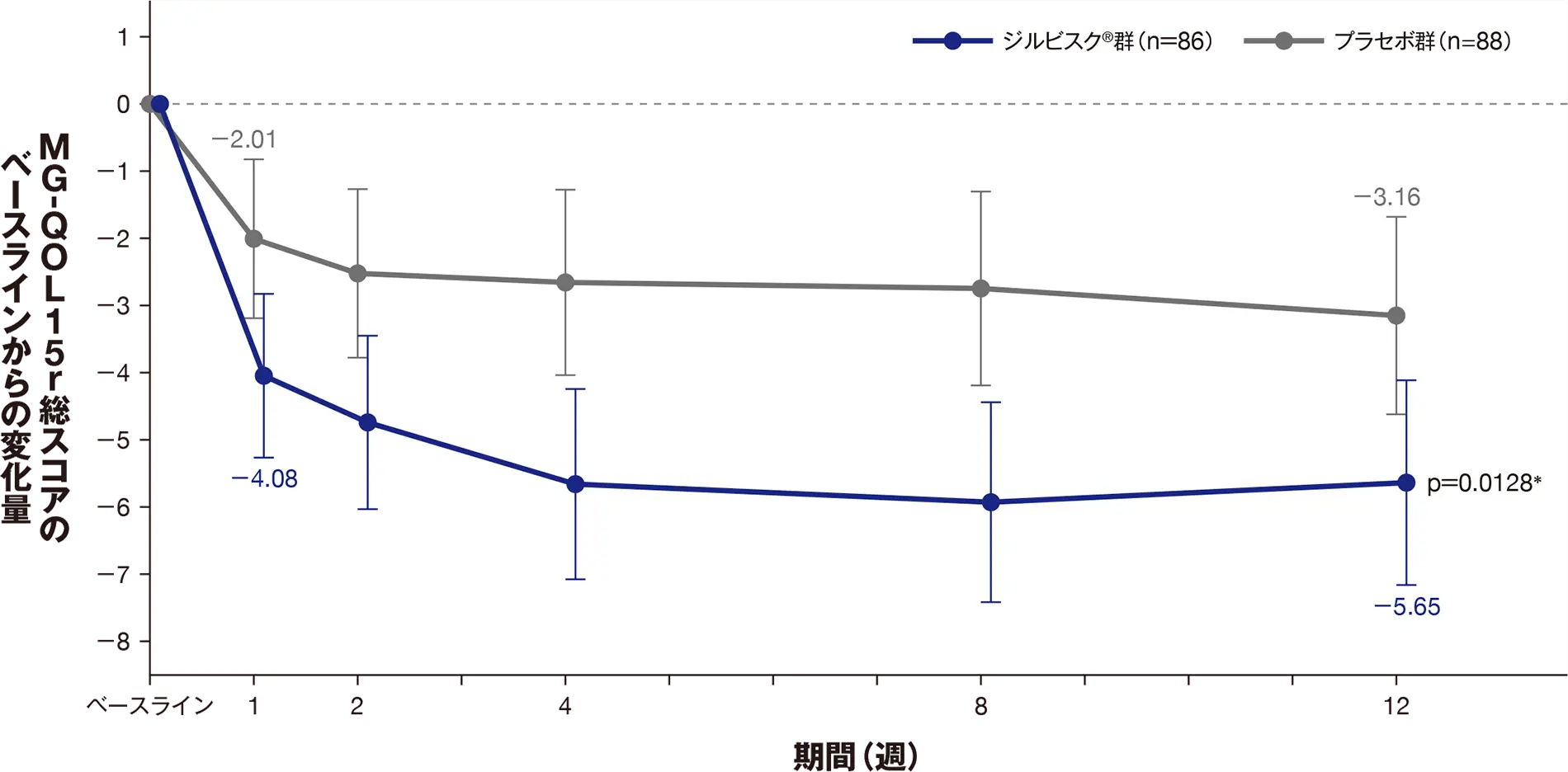
重要な副次評価項目:12週におけるMG-QOL15r総スコアのベースラインからの変化量
12週におけるMG-QOL15r総スコアのベースラインからの変化量のLS平均値は、ジルビスクⓇ群-5.65、プラセボ群-3.16であり、ジルビスクⓇ群でプラセボに対して統計学的に有意な低下が見られました[LS平均値の差:-2.49、p=0.0128(MMRM ANCOVAモデル解析)]。
ジルビスクⓇ群では、投与1週からMG-QOL15r総スコアの低下がみられました[ベースラインからの変化量のLS平均値(95%CI):-4.08(-5.30~-2.85)]。
| ジルビスクⓇ群(n=86) | プラセボ群(n=88) | |
|---|---|---|
| LS平均値±SE(95%CI) | -5.65±0.77(-7.17~-4.12) | -3.16±0.76(-4.65~-1.67) |
| LS平均値の群間差±SE(95%CI) | -2.49±0.99(-4.45~-0.54) | ― |
| p値 | 0.0128* | ― |
- *
- 治験薬、治験薬と来院の交互作用項、ベースラインのMG-ADL、QMG及びMG-QOL15r総スコア、地理的地域、並びにベースラインのMG-QOL15r総スコアと来院の交互作用項を固定効果、患者を変量効果としたMMRM ANCOVAモデル解析
- *
- 治験薬、治験薬と来院の交互作用項、ベースラインのMG-ADL、QMG及びMG-QOL15r総スコア、地理的地域、並びにベースラインのMG-QOL15r総スコアと来院の交互作用項を固定効果、患者を変量効果としたMMRM ANCOVAモデル解析
本剤の用法及び用量、用法及び用量に関連する注意等は以下の通り(電子添文から抜粋)
- 6.
-
用法及び用量
通常、成人にはジルコプランとして下表に示す用量を1日1回皮下投与する。
体重 投与量 56kg未満 16.6mg 56kg以上77kg未満 23.0mg 77kg以上 32.4mg - 7.
-
用法及び用量に関連する注意
本剤投与開始12週後までに症状の改善が認められない患者では、他の治療法への切り替えを考慮すること。
- 9.
-
特定の背景を有する患者に関する注意(抜粋)
- 9.5
-
妊婦
妊婦又は妊娠している可能性のある女性には、治療上の有益性が危険性を上回ると判断される場合にのみ投与すること。
- 9.6
-
授乳婦
治療上の有益性及び母乳栄養の有益性を考慮し、授乳の継続又は中止を検討すること。
- 1
- Wolfe GI et al.: Neurology. 1999; 52(7): 1487-1489.
- 2
- Muppidi S et al.: Muscle Nerve. 2011; 44(5): 727-731.
- 3
- Barnett C et al.: J Clin Neuromuscul Dis. 2012; 13(4): 201-205.
- 4
- Barohn RJ et al.: Ann N Y Acad Sci. 1998; 841: 769-772.
- 5
- Barnett C et al.: Neurol Clin. 2018; 36(2): 339-353.
- 6
- Thomsen JLS et al.: Front Neurol. 2020; 11: 596382.
- 7
- Burns TM et al.: Neurology. 2010; 74(18): 1434-1440.